纳米抗体研发的“神助攻”——无细胞蛋白表达(CFPS)技术
2025-01-06

当今生物医学研究正进入亚细胞层面,这得益于纳米医学、纳米诊断和纳米治疗的迅猛发展,同时纳米粒子在疾病预防、诊断、治疗和后续追踪中也得到了广泛应用。纳米抗体作为一种新型且独特的抗原结合片段,因其具有体积小、稳定性高、抗原结合亲和力强、水溶性好以及来源于自然等优越特性,正成为开发新一代生物药物的热门选择。目前,多个纳米抗体已进入临床研究阶段,为治疗各种人类疾病提供了新的可能性。然而,纳米抗体的筛选和功能验证过程往往繁琐且耗时。近年来,无细胞蛋白表达(CFPS)技术的快速发展为纳米抗体的研发带来了新的机遇。
一、纳米抗体及其筛选与功能验证
纳米抗体(Nanobody,Nbs)也称为基于单域的重链抗体可变区抗体片段,是来自Camelidae科中发现的仅重链IgG抗体的抗体片段。多年来,纳米抗体在各种研究领域一直备受关注,特别是在疾病的诊断和治疗方面。世界上第一种基于纳米体的药物(Caplacizumab)在2018年获得批准,此后不久又批准了其他药物。相比于传统抗体,纳米抗体有更多优势:1. 特异性、组织穿透力更强;2. 稳定性高,如耐高温;3. 更加适合工业化大规模生产;更容易改造和优化等。

图1:生成纳米抗体的方法、表征和可能的应用的示意图
纳米抗体的筛选和功能验证是纳米抗体研发过程中的关键环节。通过筛选,可以从大量的候选抗体中挑选出具有高亲和力和特异性的抗体;而功能验证则是确保所选抗体能够在实际应用中发挥预期作用的重要步骤。这两个过程都需要大量的蛋白表达和纯化工作,因此,快速且高效的蛋白表达系统对于加速纳米抗体的研发至关重要。
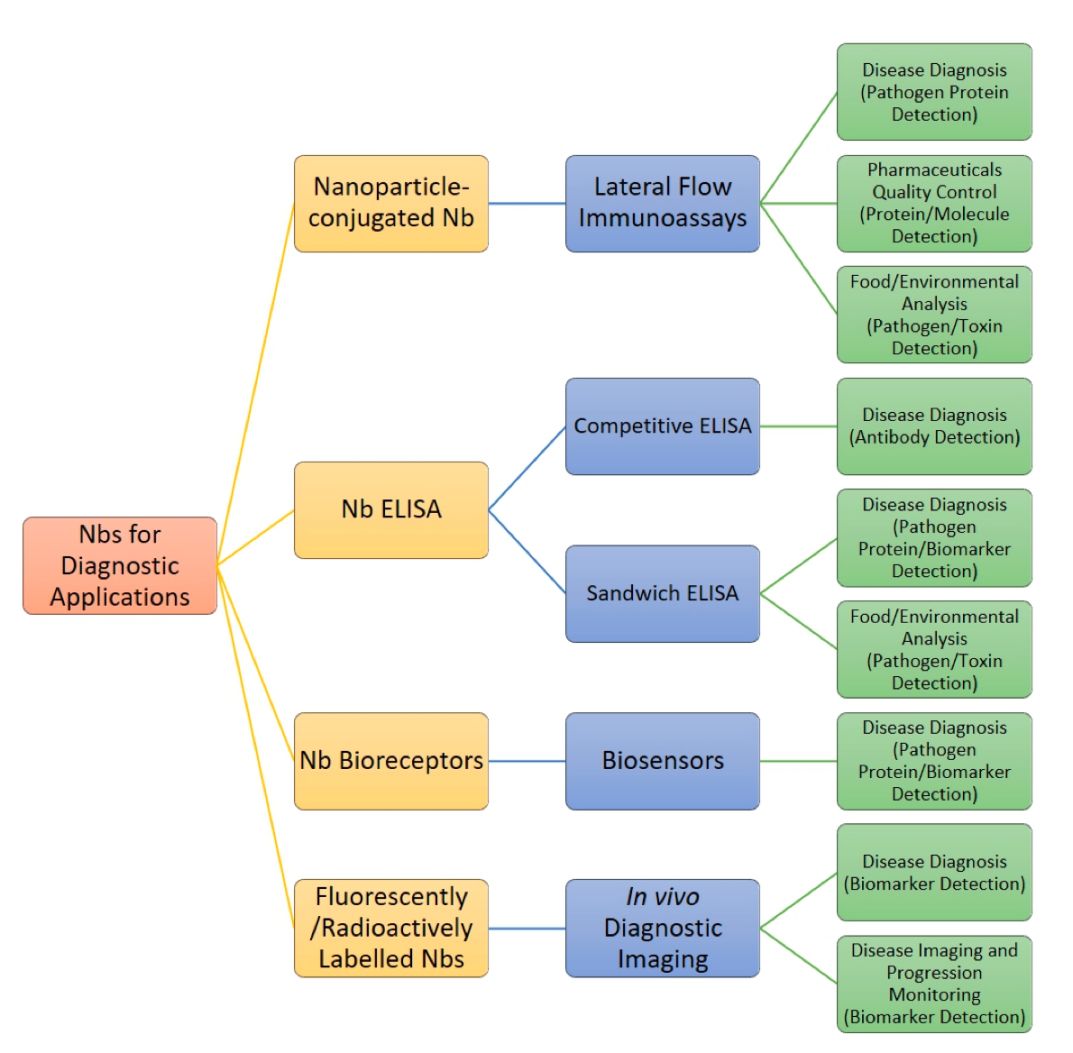
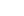
图2:纳米抗体用于诊断的流程图
二. CFPS技术在纳米抗体筛选和功能验证上的优势
相较于传统的细胞内表达系统,CFPS系统在纳米抗体的筛选和功能验证上具有多方面的优势:
1.能够在极短的时间内产生大量的目标蛋白,从而大大缩短了实验周期。传统的蛋白表达过程可能需要2至3天的时间,而CFPS系统则可以将这一时间缩短到1至2小时;
2.能够提供高产量的蛋白质合成,并且不涉及复杂的细胞内调控机制,可以更容易地控制反应条件,从而提高特定蛋白质的表达水平和质量;
3.支持高通量筛选,这使得研究人员可以在短时间内从庞大的候选抗体库中快速识别出具有潜在应用价值的纳米抗体。特别适用于纳米抗体的初步筛选,可以显著减少所需的实验时间和成本。
4.在功能验证方面,由于无细胞系统是一个开放式反应,研究人员可以更容易地控制实验条件,进行详细的生物活性测试,如亲和力、稳定性和特异性等。这对于确保纳米抗体在实际应用中的有效性和安全性是非常重要的。
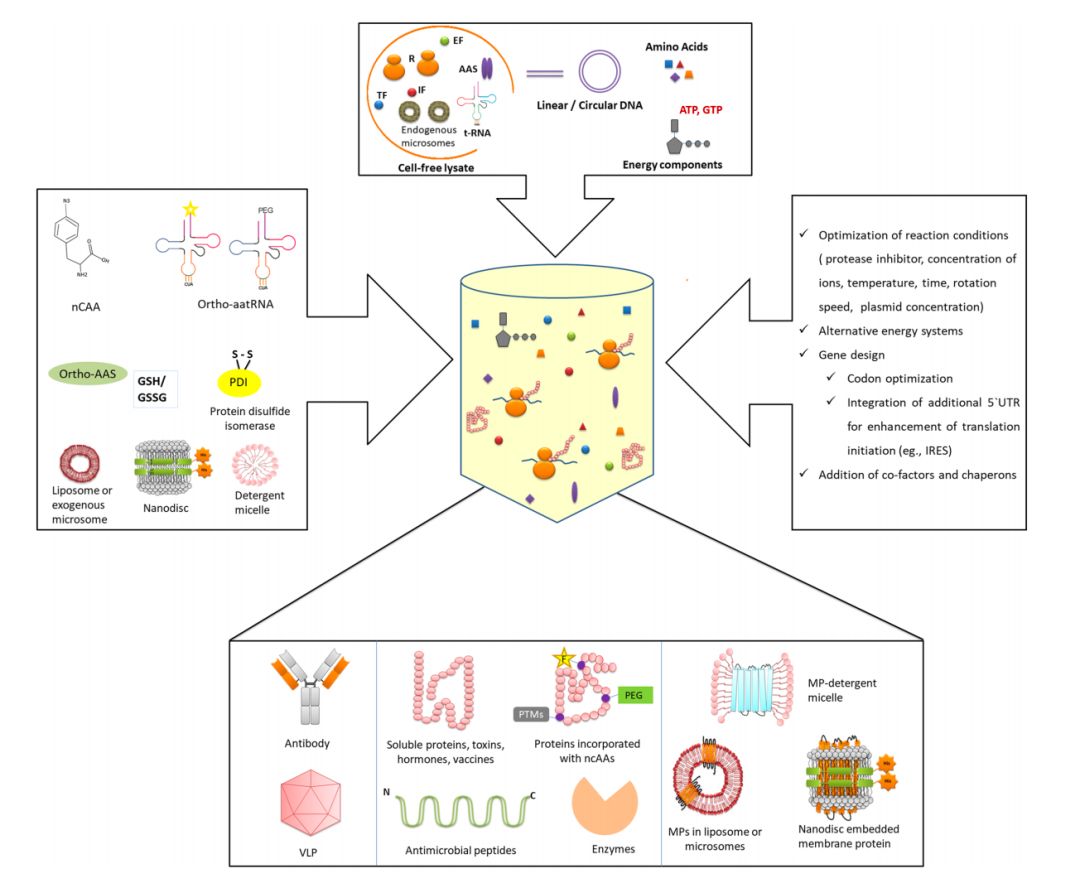
图3:无细胞生产的一般过程
总之,无细胞蛋白表达技术在纳米抗体的筛选和功能验证上提供了高效率、高产量、高通量以及易于控制的实验条件等多方面的优势,这些优势极大地推动了纳米抗体研发的进程和成功率,使其成为现代生物医药研究中的一个重要工具。
三、案例分享
近年来,越来越多的研究证明了CFPS在纳米抗体研发中的巨大潜力。Krebs SK, Stech M等人报道了在大肠杆菌和CHO无细胞系统中可产生具有活性的重组免疫毒素(RIT),并验证了CFPS允许在时间高效的工作流程中按需测试抗体-毒素结合活性,而无需细胞溶解或纯化。
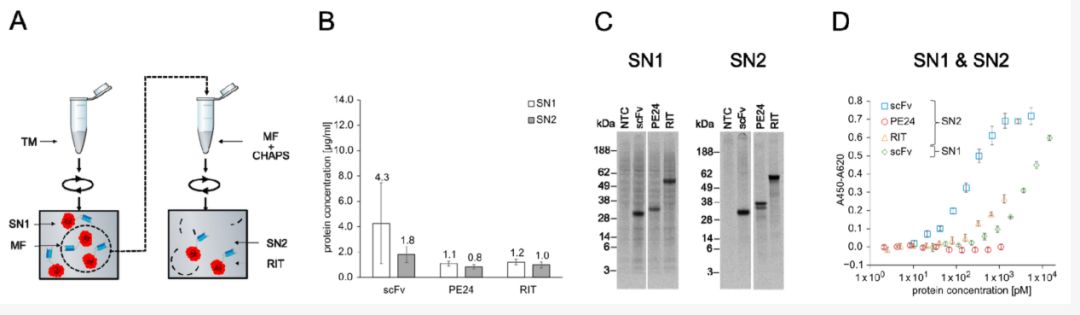
图4:大肠杆菌无细胞生产的蛋白质与GroEL/GroES伴侣的定量、自体造影和抗原结合
另一项研究中,Ding R, Hung KC等人使用杂交瘤细胞混合物来表征系统,利用液滴技术进行分类,结合CFPS技术从14个分类细胞中生成单链可变片段格式(scFv)抗体。其中12个显示了ELISA的抗原特异性结合。
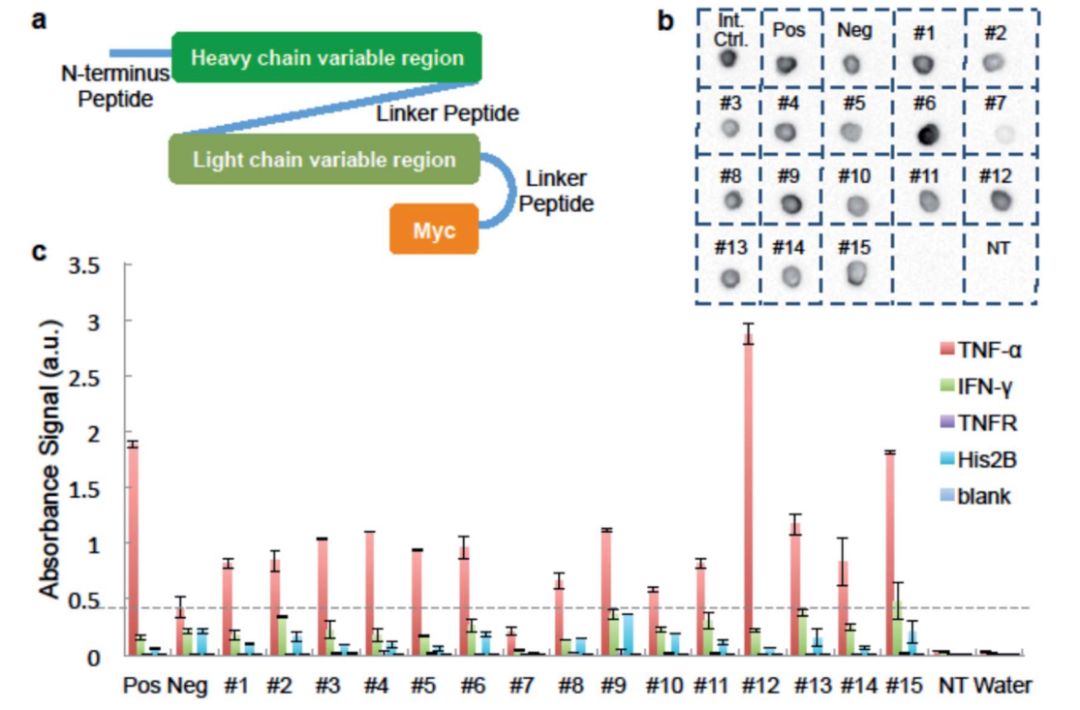
图5:分离抗体序列分析
四、结论
CFPS技术的快速发展为纳米抗体的筛选和功能验证带来了巨大的便利。其快速表达的特点不仅缩短了研发周期,还提高了筛选的效率和准确性。随着这一技术的不断优化和完善,相信未来在生物医药领域,特别是纳米抗体的研发中,无细胞表达技术将发挥更加重要的作用。为人类的健康事业贡献更多的力量。


珀罗汀生物—每个实验室都应该有个蛋白表达急救包!
参考文献:
Jovčevska I, Muyldermans S. The Therapeutic Potential of Nanobodies. BioDrugs. 2020;34(1):11-26. doi:10.1007/s40259-019-00392-z.
Jin BK, Odongo S, Radwanska M, Magez S. Nanobodies: A Review of Generation, Diagnostics and Therapeutics. Int J Mol Sci. 2023;24(6):5994. Published 2023 Mar 22. doi:10.3390/ijms24065994.
Muyldermans S. Applications of Nanobodies. Annu Rev Anim Biosci. 2021;9:401-421. doi:10.1146/annurev-animal-021419-083831.
Krebs SK, Stech M, Jorde F, et al. Synthesis of an Anti-CD7 Recombinant Immunotoxin Based on PE24 in CHO and E. coli Cell-Free Systems. Int J Mol Sci. 2022;23(22):13697. Published 2022 Nov 8. doi:10.3390/ijms232213697.
Dondapati SK, Stech M, Zemella A, Kubick S. Cell-Free Protein Synthesis: A Promising Option for Future Drug Development. BioDrugs. 2020;34(3):327-348. doi:10.1007/s40259-020-00417-y.
Krebs SK, Stech M, Jorde F, et al. Synthesis of an Anti-CD7 Recombinant Immunotoxin Based on PE24 in CHO and E. coli Cell-Free Systems. Int J Mol Sci. 2022;23(22):13697. Published 2022 Nov 8. doi:10.3390/ijms232213697.
Ding R, Hung KC, Mitra A, et al. Rapid isolation of antigen-specific B-cells using droplet microfluidics. RSC Adv. 2020;10(45):27006-27013. Published 2020 Jul 20. doi:10.1039/d0ra04328a.